
一、實驗目的和要求
自臭氧應用于水處理以來,在實際應用中取得了明顯的成效。但臭氧氧化反應具有一定的選擇性,氧化產物常常為小分子羧酸,酮和醛類物質,難以將有機物徹底降解為CO2、H2O 或其它無機物,因此TOC 和CODcr 去除率不是很高。
為了強化臭氧處理效果,人們開發出O3/UV、O3/H2O2/UV、O3/固體催化劑(如活性炭,金屬及其氧化物)等高級氧化技術,其共同特征是產生高活性羥基自由基(·OH),從而達到徹底降解有機污染物的目的。影響臭氧氧化的因素有污染物成分、含量,臭氧投加量,廢水pH,水氣接觸時間,紫外波長,照射強度,氣體分布狀況,水溫等。
本實驗希望達到下述目的:①加深對臭氧氧化法處理廢水機理的理解;
②掌握臭氧氧化法處理廢水的最佳條件試驗方法。
二、實驗內容和原理
臭氧氧化能力很強,O3+2H++2e→O2+H2O反應體系的標準電極電位E=2.07V。臭氧在水中分解產生原子氧和氧氣還可以產生一系列自由基,其反應式如下:
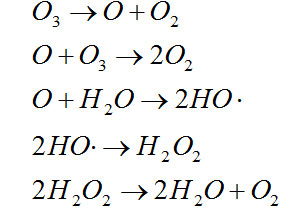
特別是在堿性介質中,O3分解產生自由基的速度很快,其反應式為:
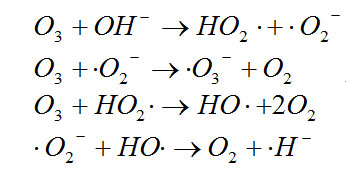
新生成的羥基自由基尤其活潑,氧化能力更強,HO﹒+Ht+e→H2O,反應體系的標準電極電位Eo=2.80V。臭氧與水中有機物的反應十分復雜,既有臭氧的直接氧化反應,也有新生自由基的氧化反應。這與反應條件與有機物的性質密切相關,酸性條件下,臭氧分解慢,O3的直接氧化反應起主要作用;堿性條件下,臭氧分解快,羥基自由基氧化作用加大,隨著溶液pH提高,CODcr去除率增加,氧化率提高。另外,溫度升高,臭氧分解速度加快,且化學反應速率提高,所以高溫有利于有機物氧化。
三、主要儀器設備裝置
常用實驗室儀器;O3反應器,剩余O3消除器;加熱-回流裝置;25mL酸式滴定管;防暴沸玻璃珠;pHS型pH計1臺;50ml燒杯若干;100ml量筒各8只,20ml、10ml移液管各1支。
蒸餾水;硫酸銀,化學純;硫酸,ρ=1.84g/mL;硫酸銀-硫酸試劑;重鉻酸鉀標準溶液(c=0.25mol/L);硫酸亞鐵銨標準滴定溶液(c=0.1006mol/L);試亞鐵靈指示劑溶液。
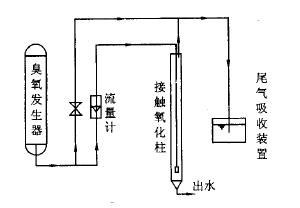
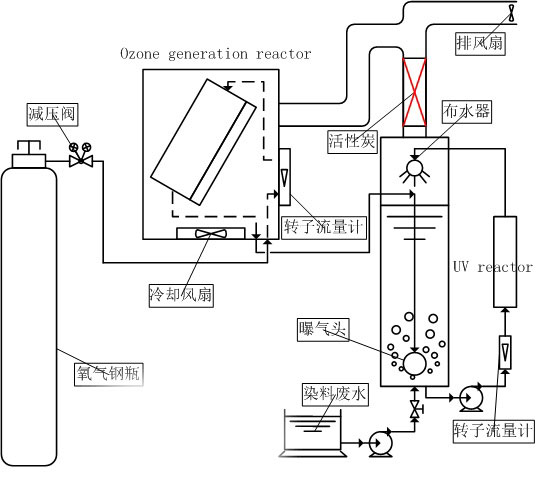
圖1 臭氧降解印染廢水研究實驗裝置
四、操作方法和實驗步驟
Ø 不同氧化時間的處理效果的實驗步驟
1、 仔細觀察O3裝置的內、外結構及部件;
2、 開啟泵,將廢水打入O3反應器,調整流量為0.3g/L,同時測定原廢水的pH、CODcr值;
3、 打開氧氣瓶和減壓閥,調整臭氧發生器的進氣流量為0.1m3/h;
4、 打開電源開關,設置放電功率為80%,使其產生穩定的臭氧濃度;
5、 經氧化反應10min、20min、30min、40min、50min后分別取一定的水樣,分別測定不同氧化時間后出水的pH、CODcr值。
6、 實驗完成后,關閉電源開關、臭氧發生器及泵,整理實驗。
Ø 水質化學需氧量測定的實驗步驟
1) 移液管取20.0mL待測試料于潔凈的250ml錐形瓶中。
2) 于試料中加入10.0mL重鉻酸鉀標準溶液和幾顆防爆沸玻璃珠,搖勻。將錐形瓶接到回流裝置冷凝管下端,接通冷凝水。從冷凝管上端緩慢加入30ml硫酸銀—硫酸試劑,以防止低沸點有機物的逸出,混合均勻后開始加熱,自溶液開始沸騰起回流1小時。
3) 充分冷卻后,用20—30mL水自冷凝管上端沖洗冷凝管2-3次,取下錐形瓶。
4) 待溶液冷卻至室溫后,加入3滴試亞鐵靈指示劑溶液,用硫酸亞鐵銨標準滴定溶液滴定,溶液的顏色由黃色經藍綠色變為紅褐色即為終點。記下硫酸亞鐵銨標準滴定溶液的消耗毫升數V2。
空白試驗:
按相同步驟以20.0ml蒸餾水代替試料進行空白試驗,記錄下空白滴定時消耗硫酸亞鐵銨標準溶液的毫升數V1。
五、實驗數據記錄和處理
表1 (NH4)2Fe(SO4)2濃度標定及空白試驗數據表
水質COD測定:
重鉻酸鉀標準溶液濃度c(1/6 K2Cr2O7)=0.2500mol/L,標定得(NH4)2Fe(SO4)2的濃度C =0.098mol/L;空白試驗所消耗的硫酸亞鐵銨標準滴定溶液的體積V1=24.65mL;試料測定所消耗的硫酸亞鐵銨標準滴定溶液的體積V2;試料的體積V0=20.00mL,則:
計算公式: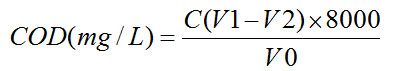
表2 直接桃紅染料廢水COD測定數據表
表3 酸性嫩黃染料廢水COD測定數據表
表4 分散藍染料廢水COD測定數據表
六、實驗結果與分析
【廢水COD及其去除率隨氧化時間變化曲線圖分析】
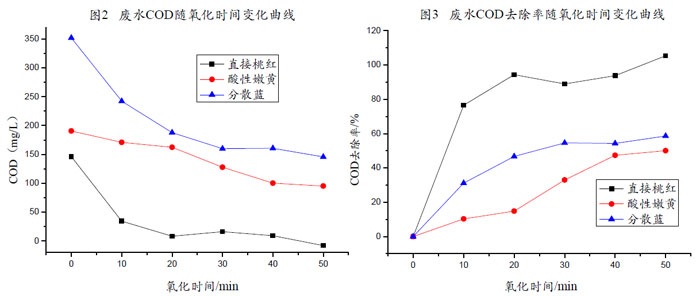
從圖2、圖3不難發現,染料廢水的COD均隨O3氧化時間的增長而降低,COD去除率則隨之逐漸增大;且臭氧對三種染料廢水的CODCr去除率有異,自圖3可發現實驗中任一氧化時間時三種染料的CODCr去除率大小為:直接桃紅>分散藍>酸性嫩黃。
CODCr的去除主要取決于有機物被氧化的程度,主要原因是染料分子結構的差異。分子反應活性越強,就越容易降解;分子結構越穩定,就越難降解。三種染料的分子結構式如圖5所示:
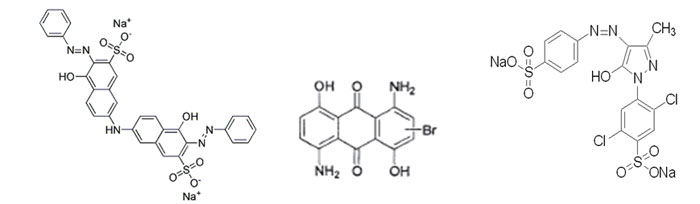 圖5 染料結構圖(從左到右分別為直接桃紅、分散藍、酸性嫩黃)
圖5 染料結構圖(從左到右分別為直接桃紅、分散藍、酸性嫩黃)
蒽醌結構的染料(如分散藍),一旦羰基被氧化打開后,整個蒽醌結構就被破壞,羰基相鄰的兩個苯環就比較容易被氧化;單偶氮結構染料(如酸性嫩黃),偶氮基(-N=N-)被氧化打開后,其相鄰的苯環及芳香環并沒有被破壞,結構相對比較穩定而不容易被氧化;雙偶氮結構的染料,有兩個偶氮基,更為穩定,被氧化的難度也就更大,所以在芳香環個數相差不大的前提下,CODcr降解效率的大小為:蒽醌結構染料>單偶氮結構染料>雙偶氮結構染料。
偏酸性和中性條件下,臭氧的氧化作用以直接氧化為主,其氧化能力較弱,選擇性較強,從各染料的分子結構中,不難發現各染料的共軛雙鍵的比重排序為:直接桃紅>分散藍>酸性嫩黃。雖然分散藍結構中氨基和羥基都是供電子基團,能夠促進染料的降解,但是羥基和氨基都可以和羰基形成分子內氫鍵,再加上吸電子基團—Br的抑制作用,染料的分子結構十分穩定而相對直接桃紅難以降解;酸性嫩黃為單偶氮結構染料,且—Cl等吸電子基團更抑制其氧化降解,故酸性嫩黃CODCr去除率最低。
最經濟反應時間點:
根據圖2、圖3,從經濟性的角度來考慮,20min、30min、40min分別是直接桃紅、分散藍和酸性嫩黃的最佳反應時間點,因為所投加的臭氧已得到最充分的利用,在各自的最佳反應時間點以后,雖然CODcr去除效率依然在不斷增加,但其增加的速度已經十分緩慢,而在臭氧的投加量不變的情況下,臭氧的利用率大大地下降,加大了經濟成本。
【廢水pH值隨氧化時間變化曲線圖分析】
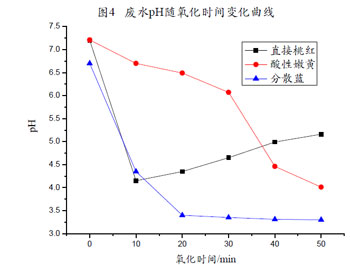
由圖4可發現,酸性嫩黃、分散藍廢水經臭氧處理后水中的pH下降,而直接桃紅除最初10min氧化處理水樣的pH相對原水樣大大降低外,之后的處理水樣隨氧化時間的增長pH稍有上升。
廢水經臭氧氧化過程中有機物不斷被氧化為小分子有機酸,酸電離產生氫離子,使水中pH下降,特別是分散藍染料廢水,有機物被臭氧氧化分解后,氫溴酸從分子結構中解離出來,經氧化后產生溴酸等強酸性的酸,所以其pH下降最為明顯。而直接桃紅的臭氧化過程是:臭氧首先攻擊與偶氮鍵相連的C—N鍵,使偶氮鍵以氮氣排出,同時分子中苯環和萘環被氧原子取代,開環后被逐步氧化成酚、醇、醛和酰胺等,然后進一步被氧化成有機酸,最后部分有機物被徹底氧化為CO2和H2O,因而在氧化得到的有機酸使水樣pH下降后,其繼續被氧化得到CO2并逸出使水樣pH又小幅度上升。
【實驗誤差來源分析】
本實驗的誤差主要來源于水質COD測定,實驗測得各水質的COD結果有部分小于50mg/L,根據環境監測原理,此部分水質的COD測定本應采用低濃度的重鉻酸鉀標準溶液(c=0.025mol/L)氧化,加熱回流足夠時間以后,采用低濃度的硫酸亞鐵銨標準溶液回滴;而本次實驗中水質COD測定統一用的重鉻酸鉀標準溶液c=0.25mol/L,濃度偏高,滴定的準確率勢必有所下降。
測定的水質COD結果誤差(如測得直接桃紅50min氧化水樣的COD<0等)來源主要有偏小的原因可能是以下幾方面:
(1) 實驗中所使用的移液管等各類儀器設備本身帶入的移取試料、試劑體積的誤差;
(2) 回流過程加入硫酸的速度沒有控制好,致使有少量低沸點有機物溢出(加硫酸時錐形瓶中有少量煙冒出,說明低沸點有機物的損失不可忽略);
(3) 考慮到試驗時間限制,回流加熱時間只有1h(本應為2小時),有機物的氧化可能不夠充分;
(4) 滴定終點的判斷誤差,依賴于實驗者觀察顏色變化的敏銳度,直接影響硫酸亞鐵標準液的濃度標定及水樣COD測定結果等;
(5) 本實驗COD測定方法的適用范圍是COD為30—700mg/L,實驗結果中直接桃紅部分水樣的COD小于30 mg/L,此部分數據存在不可忽略的實驗誤差。
七、討論、心得
u 本實驗的關鍵是水質COD的測定;為減少操作帶入的實驗誤差,水質COD測定應注意如下事項:
1) 本實驗測量使用原水樣,不需過濾;取樣時應先放掉一部分染料水樣,排除留在取樣口處的水樣,因為這部分水樣時沒有被處理的,否則將造成實驗誤差;
2) 為保證實驗數據的精密度,廢水取樣、各試劑的加入及滴定等同類操作應盡量由同一人完成;
3) 本方法的適用范圍是COD大于30 mg/L 小于700mg/L,計算結果COD值小于10mg/L時,應表示為“COD<10mg/L”;若測出的值超出700mg/L,水樣必須經稀釋后再測定;
4) 滴定實驗中,滴定終點的判斷非常重要;滴定時要不斷旋動錐形瓶,時刻注意瓶中溶液顏色的轉變;在酸性重鉻酸鉀條件下,芳烴及吡啶難以被氧化,其氧化率較低。在硫酸銀催化作用下,直鏈脂肪族化合物可有效地被氧化,所以此方法的準確度不是100%;
5) 硫酸要在裝好冷凝管,通好冷凝水之后再緩緩由冷凝管上部加入,要控制加入速度,不宜過快,目的是為了防止低沸點有機物的溢出;
6) 無機還原性物質如亞硝酸鹽、硫化物及二價鐵鹽將使結果增加,將其需氧量作為水樣COD值的一部分是可以接受的。該實驗的主要干擾物為氯化物,可加入硫酸汞部分地消除干擾,經回流后,氯離子可與硫酸汞結合成可溶性的氯汞絡合物。
7) 對于污染嚴重的水樣,可選取所需體積1/10的試料和1/10的試劑,放入10×150mm硬質玻璃管中,搖勻后,用酒精燈加熱至沸數分鐘,觀察溶液是否變成藍綠色。如呈藍綠色,應再適當少取試料,重復以上試驗,直至溶液不變藍綠色為止。從而確定待測水樣適當的稀釋倍數。
u 臭氧濃度過高會對人體造成不利的影響:臭氧濃度高于0.3mg/L時對人的五官有刺激作用;濃度高于3-15mg/L時,人會感到頭疼,所以一般臭氧的濃度允許值為0.2mg/L,正常可與人體接觸8小時;采用臭氧氧化技術也應該注意剩余臭氧的去除,主要方法有:
i. 預臭氧化:將剩余臭氧重新通入待處理的廢水中,可達到循環使用的目的。
ii. 稀釋:對排出的臭氧進行一定的稀釋,使得臭氧對人體的危害減小。
iii. 熱分解:臭氧在100℃時分解反應很劇烈,在270℃時基本沒有臭氧的存在。
iv. 吸附:可以采用碘酸鉀等物質對臭氧進行吸附去除。
八、思考題:
1、為什么臭氧氧化對TOC的去除效率不是很高?
答:處理液的pH為酸性的情況下,臭氧氧化的選擇性較高且反應較慢;處理液pH為堿性的條件下,臭氧氧化分解產生的CO2又被堿性溶液吸收,故臭氧氧化對TOC的去除率不高。
2、為什么廢水在強堿性時其TOC的去除效率反而下降?
答: 隨著廢水pH的增大,有機物被臭氧氧化產生的CO2極易被堿性溶液吸收,產生CO32-及HCO3-,而這兩種離子的存在會抑制羥基自由基的產生,進而抑制有機物氧化作用,所以隨著廢水pH的升高(強堿性),其TOC的去除率反而變小。
3、化學氧化技術還有哪些方法?
答: 目前常用的化學氧化法根據氧化劑的種類分為有臭氧氧化、Fenton氧化、氯氧化、光催化氧化、濕氣氧化法等;根據技術發展的進展可以分為傳統氧化法和高新技術氧化法。
臭氧氧化法:臭氧是良好的強氧化脫色劑,對于大多數染料能獲得良好的脫色效果,但對于其他以細分散SS狀態存在于廢水中的還原、硫化和涂料等不溶水染料脫色效果差。實際中常和其他方法聯合使用,與紫外光輻射或活性炭吸附聯合處理,可提高脫色效果;臭氧-電解處理可提高酸性染料、堿性和活性染料的脫色率。從國內外運行經驗和結果來看,由于臭氧氧化不產生污泥和二次污染,有一定的工業應用前景;但處理成本高,不適合大流量廢水的處理。
氯氧化法:常用的氯氧化劑有液氯、漂白粉、次氯酸鈉和二氧化氯等,氯氧化劑對于易氧化的水溶性染料,如陽離子染料和硫化染料有較好的脫色效果;對于不易氧化的水不溶性染料,如還原、分散染料等脫色效果較差;當廢水中含有較多SS和漿料時,氯氧化法去除效果不理想。
Fenton法:Fenton試劑對含染料廢水進行混凝前的預處理,脫色率可達96.77%。近年來人們把UV、草酸鹽引入Fenton工藝中,使其氧化能力大大增強,但處理毒性大。一般處理氧化物或生物難降解的有機廢水時,與混凝沉降、活性炭、生物法等連用,可降低處理成本。
光催化氧化法:常用的催化劑有TiO2、H2O2、草酸鐵等無機試劑,TiO2由于無毒、有較高的催化能力和較好的化學穩定性,成為應用最廣泛的光催化劑;利用太陽能進行光催化氧化有機染料技術,在節約能源、維持生態平衡、實現可持續發展等方面具有突出的優點。光催化氧化技術的一個新的發展方向——電化學催化氧化降解技術即光電催化,利用光透電極和結構TiO2作為工作電極和光催化劑,對水中染料進行電解,發現光電催化劑對3種染料——品紅、鉻藍K、鉻黑T溶液的降解效果最佳。
超臨界氧化法(SCWO):超臨界氧化法(SCWO)指當溫度、壓力高于水的臨界溫度374℃和臨界壓力22.05MPa條件下的水中有機物的氧化。Model等對有機碳含量27.33g/L的有機廢水,在550℃、60s內,有機碳和有機氯的去除率分別為99.99%和99.97%。SCWO具有效率高、應速度快、適用范圍廣特點,除有機污染物的同時,可提高生化降解性。
高級氧化法:如UV+H2O2、UV+O3,在氧化過程中產生羥基自由基(·OH),其強氧化性使染料廢水脫色。經研究發現它對偶氮染料的脫色很有效,高級氧化反應隨O3和H2O2加入量的增加,其反應速率也隨之增加。在實際生產中加入某些化學輔助劑會提高脫色效果,最近的研究發現二氯三嗪基型偶氮類活性染料使用UV+H2O2方法脫色也有很好的效果。
自臭氧應用于水處理以來,在實際應用中取得了明顯的成效。但臭氧氧化反應具有一定的選擇性,氧化產物常常為小分子羧酸,酮和醛類物質,難以將有機物徹底降解為CO2、H2O 或其它無機物,因此TOC 和CODcr 去除率不是很高。
為了強化臭氧處理效果,人們開發出O3/UV、O3/H2O2/UV、O3/固體催化劑(如活性炭,金屬及其氧化物)等高級氧化技術,其共同特征是產生高活性羥基自由基(·OH),從而達到徹底降解有機污染物的目的。影響臭氧氧化的因素有污染物成分、含量,臭氧投加量,廢水pH,水氣接觸時間,紫外波長,照射強度,氣體分布狀況,水溫等。
本實驗希望達到下述目的:①加深對臭氧氧化法處理廢水機理的理解;
②掌握臭氧氧化法處理廢水的最佳條件試驗方法。
二、實驗內容和原理
臭氧氧化能力很強,O3+2H++2e→O2+H2O反應體系的標準電極電位E=2.07V。臭氧在水中分解產生原子氧和氧氣還可以產生一系列自由基,其反應式如下:
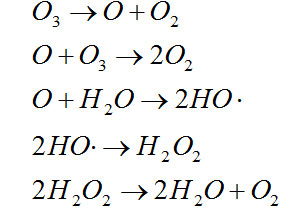
特別是在堿性介質中,O3分解產生自由基的速度很快,其反應式為:
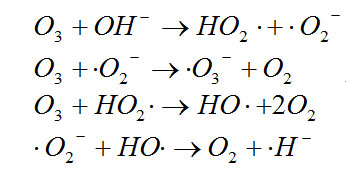
新生成的羥基自由基尤其活潑,氧化能力更強,HO﹒+Ht+e→H2O,反應體系的標準電極電位Eo=2.80V。臭氧與水中有機物的反應十分復雜,既有臭氧的直接氧化反應,也有新生自由基的氧化反應。這與反應條件與有機物的性質密切相關,酸性條件下,臭氧分解慢,O3的直接氧化反應起主要作用;堿性條件下,臭氧分解快,羥基自由基氧化作用加大,隨著溶液pH提高,CODcr去除率增加,氧化率提高。另外,溫度升高,臭氧分解速度加快,且化學反應速率提高,所以高溫有利于有機物氧化。
三、主要儀器設備裝置
常用實驗室儀器;O3反應器,剩余O3消除器;加熱-回流裝置;25mL酸式滴定管;防暴沸玻璃珠;pHS型pH計1臺;50ml燒杯若干;100ml量筒各8只,20ml、10ml移液管各1支。
蒸餾水;硫酸銀,化學純;硫酸,ρ=1.84g/mL;硫酸銀-硫酸試劑;重鉻酸鉀標準溶液(c=0.25mol/L);硫酸亞鐵銨標準滴定溶液(c=0.1006mol/L);試亞鐵靈指示劑溶液。

圖1 臭氧降解印染廢水研究實驗裝置
四、操作方法和實驗步驟
Ø 不同氧化時間的處理效果的實驗步驟
1、 仔細觀察O3裝置的內、外結構及部件;
2、 開啟泵,將廢水打入O3反應器,調整流量為0.3g/L,同時測定原廢水的pH、CODcr值;
3、 打開氧氣瓶和減壓閥,調整臭氧發生器的進氣流量為0.1m3/h;
4、 打開電源開關,設置放電功率為80%,使其產生穩定的臭氧濃度;
5、 經氧化反應10min、20min、30min、40min、50min后分別取一定的水樣,分別測定不同氧化時間后出水的pH、CODcr值。
6、 實驗完成后,關閉電源開關、臭氧發生器及泵,整理實驗。
Ø 水質化學需氧量測定的實驗步驟
1) 移液管取20.0mL待測試料于潔凈的250ml錐形瓶中。
2) 于試料中加入10.0mL重鉻酸鉀標準溶液和幾顆防爆沸玻璃珠,搖勻。將錐形瓶接到回流裝置冷凝管下端,接通冷凝水。從冷凝管上端緩慢加入30ml硫酸銀—硫酸試劑,以防止低沸點有機物的逸出,混合均勻后開始加熱,自溶液開始沸騰起回流1小時。
3) 充分冷卻后,用20—30mL水自冷凝管上端沖洗冷凝管2-3次,取下錐形瓶。
4) 待溶液冷卻至室溫后,加入3滴試亞鐵靈指示劑溶液,用硫酸亞鐵銨標準滴定溶液滴定,溶液的顏色由黃色經藍綠色變為紅褐色即為終點。記下硫酸亞鐵銨標準滴定溶液的消耗毫升數V2。
空白試驗:
按相同步驟以20.0ml蒸餾水代替試料進行空白試驗,記錄下空白滴定時消耗硫酸亞鐵銨標準溶液的毫升數V1。
五、實驗數據記錄和處理
表1 (NH4)2Fe(SO4)2濃度標定及空白試驗數據表
| (NH4)2Fe(SO4)2濃度標定實驗 | (NH4)2Fe(SO4)2用量/ml | (NH4)Fe(SO4)2濃度 |
| 25.42 | 0.098mol/L | |
| 25.50 | ||
| 全程空白實驗 | 24.61 | 24.65 |
| 24.90 | ||
| 24.45 |
重鉻酸鉀標準溶液濃度c(1/6 K2Cr2O7)=0.2500mol/L,標定得(NH4)2Fe(SO4)2的濃度C =0.098mol/L;空白試驗所消耗的硫酸亞鐵銨標準滴定溶液的體積V1=24.65mL;試料測定所消耗的硫酸亞鐵銨標準滴定溶液的體積V2;試料的體積V0=20.00mL,則:
計算公式:
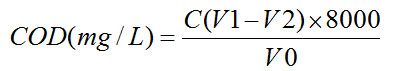
表2 直接桃紅染料廢水COD測定數據表
| 水樣 | pH值 |
硫酸亞鐵銨的 滴定消耗量(mL) |
COD (mg/L) | COD去除率(%) |
| 原水樣(0 min) | 7.20 | 20.89 | 146.27 | 0.0 |
| 10 min水樣 | 4.15 | 23.74 | 34.21 | 76.6 |
| 20 min水樣 | 4.35 | 24.40 | 8.26 | 94.4 |
| 30 min水樣 | 4.65 | 24.20 | 16.12 | 89.0 |
| 40 min水樣 | 4.99 | 24.38 | 9.04 | 93.8 |
| 50 min水樣 | 5.16 | 24.81 | -7.86 | 105.4 |
| 水樣 | pH值 |
硫酸亞鐵銨的 滴定消耗量(mL) |
COD (mg/L) | COD去除率(%) |
| 原水樣(0 min) | 7.21 | 19.60 | 190.70 | 0.0 |
| 10 min水樣 | 6.70 | 20.10 | 171.04 | 10.3 |
| 20 min水樣 | 6.49 | 20.32 | 162.39 | 14.8 |
| 30 min水樣 | 6.07 | 21.20 | 127.79 | 33.0 |
| 40 min水樣 | 4.46 | 21.90 | 100.27 | 47.4 |
| 50 min水樣 | 4.01 | 22.03 | 95.15 | 50.1 |
| 水樣 | pH值 |
硫酸亞鐵銨的 滴定消耗量(mL) |
COD (mg/L) | COD去除率(%) |
| 原水樣(0 min) | 6.70 | 15.92 | 352.02 | 0.0 |
| 10 min水樣 | 4.35 | 18.72 | 242.26 | 31.2 |
| 20 min水樣 | 3.40 | 20.11 | 187.77 | 46.7 |
| 30 min水樣 | 3.35 | 20.82 | 159.94 | 54.6 |
| 40 min水樣 | 3.31 | 20.80 | 160.72 | 54.3 |
| 50 min水樣 | 3.30 | 21.18 | 145.82 | 58.6 |


六、實驗結果與分析
【廢水COD及其去除率隨氧化時間變化曲線圖分析】
從圖2、圖3不難發現,染料廢水的COD均隨O3氧化時間的增長而降低,COD去除率則隨之逐漸增大;且臭氧對三種染料廢水的CODCr去除率有異,自圖3可發現實驗中任一氧化時間時三種染料的CODCr去除率大小為:直接桃紅>分散藍>酸性嫩黃。
CODCr的去除主要取決于有機物被氧化的程度,主要原因是染料分子結構的差異。分子反應活性越強,就越容易降解;分子結構越穩定,就越難降解。三種染料的分子結構式如圖5所示:

蒽醌結構的染料(如分散藍),一旦羰基被氧化打開后,整個蒽醌結構就被破壞,羰基相鄰的兩個苯環就比較容易被氧化;單偶氮結構染料(如酸性嫩黃),偶氮基(-N=N-)被氧化打開后,其相鄰的苯環及芳香環并沒有被破壞,結構相對比較穩定而不容易被氧化;雙偶氮結構的染料,有兩個偶氮基,更為穩定,被氧化的難度也就更大,所以在芳香環個數相差不大的前提下,CODcr降解效率的大小為:蒽醌結構染料>單偶氮結構染料>雙偶氮結構染料。
偏酸性和中性條件下,臭氧的氧化作用以直接氧化為主,其氧化能力較弱,選擇性較強,從各染料的分子結構中,不難發現各染料的共軛雙鍵的比重排序為:直接桃紅>分散藍>酸性嫩黃。雖然分散藍結構中氨基和羥基都是供電子基團,能夠促進染料的降解,但是羥基和氨基都可以和羰基形成分子內氫鍵,再加上吸電子基團—Br的抑制作用,染料的分子結構十分穩定而相對直接桃紅難以降解;酸性嫩黃為單偶氮結構染料,且—Cl等吸電子基團更抑制其氧化降解,故酸性嫩黃CODCr去除率最低。
最經濟反應時間點:
根據圖2、圖3,從經濟性的角度來考慮,20min、30min、40min分別是直接桃紅、分散藍和酸性嫩黃的最佳反應時間點,因為所投加的臭氧已得到最充分的利用,在各自的最佳反應時間點以后,雖然CODcr去除效率依然在不斷增加,但其增加的速度已經十分緩慢,而在臭氧的投加量不變的情況下,臭氧的利用率大大地下降,加大了經濟成本。
【廢水pH值隨氧化時間變化曲線圖分析】
由圖4可發現,酸性嫩黃、分散藍廢水經臭氧處理后水中的pH下降,而直接桃紅除最初10min氧化處理水樣的pH相對原水樣大大降低外,之后的處理水樣隨氧化時間的增長pH稍有上升。
廢水經臭氧氧化過程中有機物不斷被氧化為小分子有機酸,酸電離產生氫離子,使水中pH下降,特別是分散藍染料廢水,有機物被臭氧氧化分解后,氫溴酸從分子結構中解離出來,經氧化后產生溴酸等強酸性的酸,所以其pH下降最為明顯。而直接桃紅的臭氧化過程是:臭氧首先攻擊與偶氮鍵相連的C—N鍵,使偶氮鍵以氮氣排出,同時分子中苯環和萘環被氧原子取代,開環后被逐步氧化成酚、醇、醛和酰胺等,然后進一步被氧化成有機酸,最后部分有機物被徹底氧化為CO2和H2O,因而在氧化得到的有機酸使水樣pH下降后,其繼續被氧化得到CO2并逸出使水樣pH又小幅度上升。
【實驗誤差來源分析】
本實驗的誤差主要來源于水質COD測定,實驗測得各水質的COD結果有部分小于50mg/L,根據環境監測原理,此部分水質的COD測定本應采用低濃度的重鉻酸鉀標準溶液(c=0.025mol/L)氧化,加熱回流足夠時間以后,采用低濃度的硫酸亞鐵銨標準溶液回滴;而本次實驗中水質COD測定統一用的重鉻酸鉀標準溶液c=0.25mol/L,濃度偏高,滴定的準確率勢必有所下降。
測定的水質COD結果誤差(如測得直接桃紅50min氧化水樣的COD<0等)來源主要有偏小的原因可能是以下幾方面:
(1) 實驗中所使用的移液管等各類儀器設備本身帶入的移取試料、試劑體積的誤差;
(2) 回流過程加入硫酸的速度沒有控制好,致使有少量低沸點有機物溢出(加硫酸時錐形瓶中有少量煙冒出,說明低沸點有機物的損失不可忽略);
(3) 考慮到試驗時間限制,回流加熱時間只有1h(本應為2小時),有機物的氧化可能不夠充分;
(4) 滴定終點的判斷誤差,依賴于實驗者觀察顏色變化的敏銳度,直接影響硫酸亞鐵標準液的濃度標定及水樣COD測定結果等;
(5) 本實驗COD測定方法的適用范圍是COD為30—700mg/L,實驗結果中直接桃紅部分水樣的COD小于30 mg/L,此部分數據存在不可忽略的實驗誤差。
七、討論、心得
u 本實驗的關鍵是水質COD的測定;為減少操作帶入的實驗誤差,水質COD測定應注意如下事項:
1) 本實驗測量使用原水樣,不需過濾;取樣時應先放掉一部分染料水樣,排除留在取樣口處的水樣,因為這部分水樣時沒有被處理的,否則將造成實驗誤差;
2) 為保證實驗數據的精密度,廢水取樣、各試劑的加入及滴定等同類操作應盡量由同一人完成;
3) 本方法的適用范圍是COD大于30 mg/L 小于700mg/L,計算結果COD值小于10mg/L時,應表示為“COD<10mg/L”;若測出的值超出700mg/L,水樣必須經稀釋后再測定;
4) 滴定實驗中,滴定終點的判斷非常重要;滴定時要不斷旋動錐形瓶,時刻注意瓶中溶液顏色的轉變;在酸性重鉻酸鉀條件下,芳烴及吡啶難以被氧化,其氧化率較低。在硫酸銀催化作用下,直鏈脂肪族化合物可有效地被氧化,所以此方法的準確度不是100%;
5) 硫酸要在裝好冷凝管,通好冷凝水之后再緩緩由冷凝管上部加入,要控制加入速度,不宜過快,目的是為了防止低沸點有機物的溢出;
6) 無機還原性物質如亞硝酸鹽、硫化物及二價鐵鹽將使結果增加,將其需氧量作為水樣COD值的一部分是可以接受的。該實驗的主要干擾物為氯化物,可加入硫酸汞部分地消除干擾,經回流后,氯離子可與硫酸汞結合成可溶性的氯汞絡合物。
7) 對于污染嚴重的水樣,可選取所需體積1/10的試料和1/10的試劑,放入10×150mm硬質玻璃管中,搖勻后,用酒精燈加熱至沸數分鐘,觀察溶液是否變成藍綠色。如呈藍綠色,應再適當少取試料,重復以上試驗,直至溶液不變藍綠色為止。從而確定待測水樣適當的稀釋倍數。
u 臭氧濃度過高會對人體造成不利的影響:臭氧濃度高于0.3mg/L時對人的五官有刺激作用;濃度高于3-15mg/L時,人會感到頭疼,所以一般臭氧的濃度允許值為0.2mg/L,正常可與人體接觸8小時;采用臭氧氧化技術也應該注意剩余臭氧的去除,主要方法有:
i. 預臭氧化:將剩余臭氧重新通入待處理的廢水中,可達到循環使用的目的。
ii. 稀釋:對排出的臭氧進行一定的稀釋,使得臭氧對人體的危害減小。
iii. 熱分解:臭氧在100℃時分解反應很劇烈,在270℃時基本沒有臭氧的存在。
iv. 吸附:可以采用碘酸鉀等物質對臭氧進行吸附去除。
八、思考題:
|

1、為什么臭氧氧化對TOC的去除效率不是很高?
答:處理液的pH為酸性的情況下,臭氧氧化的選擇性較高且反應較慢;處理液pH為堿性的條件下,臭氧氧化分解產生的CO2又被堿性溶液吸收,故臭氧氧化對TOC的去除率不高。
2、為什么廢水在強堿性時其TOC的去除效率反而下降?
答: 隨著廢水pH的增大,有機物被臭氧氧化產生的CO2極易被堿性溶液吸收,產生CO32-及HCO3-,而這兩種離子的存在會抑制羥基自由基的產生,進而抑制有機物氧化作用,所以隨著廢水pH的升高(強堿性),其TOC的去除率反而變小。
3、化學氧化技術還有哪些方法?
答: 目前常用的化學氧化法根據氧化劑的種類分為有臭氧氧化、Fenton氧化、氯氧化、光催化氧化、濕氣氧化法等;根據技術發展的進展可以分為傳統氧化法和高新技術氧化法。
臭氧氧化法:臭氧是良好的強氧化脫色劑,對于大多數染料能獲得良好的脫色效果,但對于其他以細分散SS狀態存在于廢水中的還原、硫化和涂料等不溶水染料脫色效果差。實際中常和其他方法聯合使用,與紫外光輻射或活性炭吸附聯合處理,可提高脫色效果;臭氧-電解處理可提高酸性染料、堿性和活性染料的脫色率。從國內外運行經驗和結果來看,由于臭氧氧化不產生污泥和二次污染,有一定的工業應用前景;但處理成本高,不適合大流量廢水的處理。
氯氧化法:常用的氯氧化劑有液氯、漂白粉、次氯酸鈉和二氧化氯等,氯氧化劑對于易氧化的水溶性染料,如陽離子染料和硫化染料有較好的脫色效果;對于不易氧化的水不溶性染料,如還原、分散染料等脫色效果較差;當廢水中含有較多SS和漿料時,氯氧化法去除效果不理想。
Fenton法:Fenton試劑對含染料廢水進行混凝前的預處理,脫色率可達96.77%。近年來人們把UV、草酸鹽引入Fenton工藝中,使其氧化能力大大增強,但處理毒性大。一般處理氧化物或生物難降解的有機廢水時,與混凝沉降、活性炭、生物法等連用,可降低處理成本。
光催化氧化法:常用的催化劑有TiO2、H2O2、草酸鐵等無機試劑,TiO2由于無毒、有較高的催化能力和較好的化學穩定性,成為應用最廣泛的光催化劑;利用太陽能進行光催化氧化有機染料技術,在節約能源、維持生態平衡、實現可持續發展等方面具有突出的優點。光催化氧化技術的一個新的發展方向——電化學催化氧化降解技術即光電催化,利用光透電極和結構TiO2作為工作電極和光催化劑,對水中染料進行電解,發現光電催化劑對3種染料——品紅、鉻藍K、鉻黑T溶液的降解效果最佳。
超臨界氧化法(SCWO):超臨界氧化法(SCWO)指當溫度、壓力高于水的臨界溫度374℃和臨界壓力22.05MPa條件下的水中有機物的氧化。Model等對有機碳含量27.33g/L的有機廢水,在550℃、60s內,有機碳和有機氯的去除率分別為99.99%和99.97%。SCWO具有效率高、應速度快、適用范圍廣特點,除有機污染物的同時,可提高生化降解性。
高級氧化法:如UV+H2O2、UV+O3,在氧化過程中產生羥基自由基(·OH),其強氧化性使染料廢水脫色。經研究發現它對偶氮染料的脫色很有效,高級氧化反應隨O3和H2O2加入量的增加,其反應速率也隨之增加。在實際生產中加入某些化學輔助劑會提高脫色效果,最近的研究發現二氯三嗪基型偶氮類活性染料使用UV+H2O2方法脫色也有很好的效果。
經典成功案例
-
單位名稱:某高校
臭氧選型:去除COD實驗
實驗內容:3S-T10 -
單位名稱:
臭氧選型:
實驗內容: -
單位名稱:某半導體公司
臭氧選型:制作高濃度臭氧水
實驗內容:3S-T10,3S-J5000,3S-J1000





